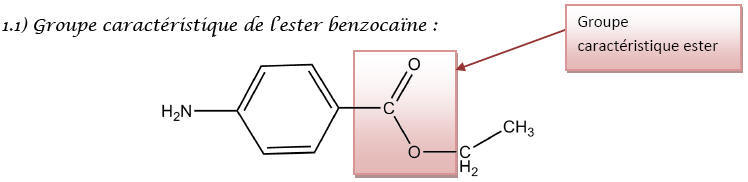
CORRIGE de Chimie (Enseignement de spécialité)
Nouvelle Calédonie - Section S - Juin 2003
Synthèse d'un médicament : la benzocaïne
I] A propos de l’aspirine
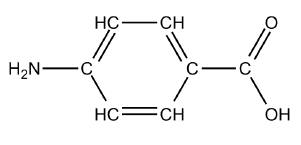
1.2) Formule semi-développée de l’acide 4-aminobenzoïque :
1.3) La réaction d’estérification est lente et limitée.
II] Quelques justifications de certaines justifications du mode opératoire.
2.1) A propos de la première étape :
2.1.1) Les ions hydronium apportés par l’acide sulfurique servent de catalyseur à la réaction. Un catalyseur permet d’augmenter la vitesse de la réaction mais ne modifie en aucun cas l’état final (quantité de produit formé). Ainsi, les ions hydronium permettent d’atteindre plus rapidement l’équilibre sans le modifier.
2.1.2) Le chauffage permet d’augmenter la vitesse de la réaction car la température est un facteur cinétique. Le réfrigérant à boules permet quant à lui de recondenser les vapeurs afin d’éviter la perte de matière.
2.1.3) Le fait d’avoir un réactif en excès permet de déplacer l’équilibre dans le sens direct (on forme plus d’ester) ainsi on augmente le rendement de la réaction.
2.2) A propos de la deuxième étape :
2.2.1) La solution de carbonate de sodium permet de purifier la phase organique. En effet, la réaction d’estérification n’est pas totale donc à la fin de la réaction il reste dans le mélange réactionnel les produits.
Or l’acide AH est très peu soluble dans l’eau donc il se trouve dans la phase organique. La solution de carbonate de sodium fait passer l’acide AH dans la phase aqueuse sous forme de 4-aminobenzoate de sodium très soluble dans l’eau.
2.2.2) L’ajout de la
solution de carbonate de sodium permet d’obtenir un
PH
voisin de 9. Donc
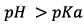 , l’espèce prédominante du couple
, l’espèce prédominante du couple
 dans le bécher après l’ajout de la solution de
carbonate de sodium est la base :
dans le bécher après l’ajout de la solution de
carbonate de sodium est la base :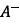 .
.
2.2.3) Le 4-aminobenzoate (de sodium) est très peu soluble dans l’eau et dans l’éthanol. En revanche, il est très soluble dans l’eau donc il se trouve majoritairement dans la phase aqueuse.
2.2.4) Ampoule à décanter :
La masse volumique de l’eau est supérieure à celle de l’éther donc la phase aqueuse est au-dessous de la phase organique :
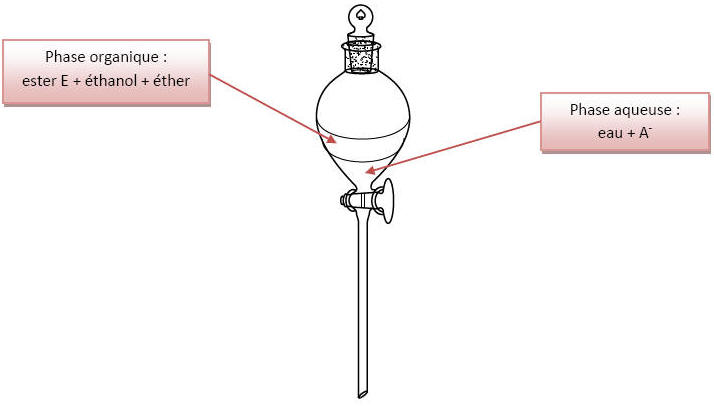
2.2.5) Le sulfate de magnésium anhydre permet d’éliminer les traces d’eau présentes dans la phase organique. La phase organique est ainsi déshydratée.
2.3) A propos de la troisième étape :
La chromatographie sur couche mince révèle deux taches pour le solide synthétisé il s’agit donc d’un mélange :
- Une tache large au niveau de celle de la benzocaïne pure.
- Une petite tache au niveau de celle de l’acide
On en déduit que le solide synthétisé contient majoritairement de la benzocaïne et un peu d’acide
AH donc il n’est pas pur.